Persamaan Keadaan Gas Ideal. Semakin rendah tekanan gas pada temperatur tetap, semakin kecil deviasinya dari perilaku ideal. Persamaan keadaan untuk gas dengan kerapatan rendah menjadi: Ρ = (mr p)/(r t) ρ = (16 x 1,52 x 10 5)/(8310 x 298) ρ = 0,98 kg/m 3. Menunjukkan kaitan p dan v pada suhu tertentu.
 Teori Gas Zainal Abidin From slideshare.net
Teori Gas Zainal Abidin From slideshare.net
Semakin tinggi tekanan gas, atau dengan dengan. Gas ideal didefinisikan sebagai gas di mana pv/nt bernilai konstan untuk seluruh keadaan. Persamaan gas ideal adalah persamaan keadaan suatu gas ideal. Ρ = m/v sehingga persamaan gas ideal menjadi. Van der walls adalah nama seorang fisikawan belanda, j. Persamaan keadaan untuk gas dengan kerapatan rendah menjadi:
Persamaan ini disebut hukum gas ideal atau persamaan keadaan gas ideal.
Jadi gas ideal memenuhi persamaan : Volume gas pada keadaan 2 (m 3) Ρ = (mr p)/(r t) ρ = (16 x 1,52 x 10 5)/(8310 x 298) ρ = 0,98 kg/m 3. Semakin rendah tekanan gas pada temperatur tetap, semakin kecil deviasinya dari perilaku ideal. P = r (t/v) pv = rt (1) dimana r adalah konstanta gas. Pada suatu gas dalam jumlah mol (n) tertentu, maka persamaan keadaan gas idealnya adalah pv = nrt
 Source: slideshare.net
Source: slideshare.net
Pv = nnakt = nrt. Pada teori kinetik gas, keadaan gas diuji oleh beberapa ilmuwan dan menghasilkan beberapa temuan sebagai berikut: Persamaaan 1 di atas disebut sebagai persamaan umum kondisi gas ideal, atau hubungan sederhana gas ideal, dan gas yang memenuhi hubungan ini disebut gas ideal. Hukum boyle dicetuskan oleh seorang ilmuwan asal inggris, yaitu robert boyle. 8.314 kj/ (kmol×k) 8.314 kpa×m3/ (kmol×k) 1.986 btu/ (lbmol×r) 1545 ft×lbf/ (lbmol×r) 10.73 psia×ft3/ (lbmol×r) jika suatu gas mengalami tekanan yang jauh lebih rendah dari tekanan kritisnya dan suhu yang jauh lebih tinggi dari suhu kritisnya maka gas tersebut dapat diperlakukan sebagai gas ideal.
 Source: gammafisblog.blogspot.com
Source: gammafisblog.blogspot.com
Tekanan gas pada keadaan 1 (n/m 2) p 2: Hukum boyle dicetuskan oleh seorang ilmuwan asal inggris, yaitu robert boyle. Persamaan gas ideal adalah persamaan keadaan suatu gas ideal. Volume gas pada keadaan 2 (m 3) Pv = nnakt = nrt.

Isometrik tekanan berbanding lurus dengan suhu. Persamaaan 1 di atas disebut sebagai persamaan umum kondisi gas ideal, atau hubungan sederhana gas ideal, dan gas yang memenuhi hubungan ini disebut gas ideal. Ρ = m/v sehingga persamaan gas ideal menjadi. Jadi gas ideal memenuhi persamaan : P = tekanan gas (n/m 2) v = volume gas (m 3) n = jumlah mol (mol) r = konstanta gas universal (r = 8,315 j/mol.k) t = suhu mutlak gas (k) catatan :
 Source: gurumuda.net
Source: gurumuda.net
Untuk gas nyata, nilai pv/nt sangat mendekati konstan sampai pada range tekanan yang besar, kita bisa melihatnya pada gambar (8.2). Pada suatu gas dalam jumlah mol (n) tertentu, maka persamaan keadaan gas idealnya adalah pv = nrt Ukuran gas tertentu p ( v−b )=rt. Persamaan keadaan gas ideal pada ruang tertutup keadaan suatu gas ideal dipengaruhi oleh tekanan, suhu, volume dan jumlah molekul gas. Tekanan gas pada keadaan 1 (n/m 2) p 2:
 Source: bagicontohsoal.blogspot.com
Source: bagicontohsoal.blogspot.com
Volume gas pada keadaan 2 (m 3) R= kna adalah konstanta gas umum, nilainya untuk semua gas adalah r = 8,314 j/mol. Persamaan ini pertama kali dicetuskan oleh émile clapeyron tahun 1834 sebagai kombinasi dari hukum boyle dan hukum charles. Tekanan gas pada keadaan 1 (n/m 2) p 2: Pertama, dalam penyelesaian soal, dirimu akan menemukan istilah stp.
 Source: slideshare.net
Source: slideshare.net
Pada persamaan ini, p adalah tekanan absolut, t adalah temperatur absolut, dan v adalah volume spesifik. Pada kondisi normal seperti temperatur dan tekanan standar ,. R= kna adalah konstanta gas umum, nilainya untuk semua gas adalah r = 8,314 j/mol. Untuk gas nyata, nilai pv/nt sangat mendekati konstan sampai pada range tekanan yang besar, kita bisa melihatnya pada gambar (8.2). Persamaan keadaan gas ideal pada ruang tertutup keadaan suatu gas ideal dipengaruhi oleh tekanan, suhu, volume dan jumlah molekul gas.
 Source: slideshare.net
Source: slideshare.net
Ternyata, ada beberapa hukum yang menjelaskan keterkaitan antara keempat besaran tersebut. P v = (m r t)/mr. Isometrik (isokhor) gas ideal keadaan v3 gas ideal yang terjadi pada volume molar sama v2. 8.314 kj/ (kmol×k) 8.314 kpa×m3/ (kmol×k) 1.986 btu/ (lbmol×r) 1545 ft×lbf/ (lbmol×r) 10.73 psia×ft3/ (lbmol×r) jika suatu gas mengalami tekanan yang jauh lebih rendah dari tekanan kritisnya dan suhu yang jauh lebih tinggi dari suhu kritisnya maka gas tersebut dapat diperlakukan sebagai gas ideal. Sebenarnya hukum avogadro menyatakan bahwa 1 mol gas ideal mempunyai volume yang sama apabila suhu dan tekanannya sama.
 Source: shareitnow.me
Source: shareitnow.me
Ternyata, ada beberapa hukum yang menjelaskan keterkaitan antara keempat besaran tersebut. Persamaan keadaan gas ideal pada ruang tertutup keadaan suatu gas ideal dipengaruhi oleh tekanan, suhu, volume dan jumlah molekul gas. Pertama, dalam penyelesaian soal, dirimu akan menemukan istilah stp. Pada persamaan ini, p adalah tekanan absolut, t adalah temperatur absolut, dan v adalah volume spesifik. Van der walls adalah nama seorang fisikawan belanda, j.
 Source: fisikasiswa.blogspot.com
Source: fisikasiswa.blogspot.com
Pada persamaan ini, p adalah tekanan absolut, t adalah temperatur absolut, dan v adalah volume spesifik. Pertama, dalam penyelesaian soal, dirimu akan menemukan istilah stp. Rumus persamaan umum gas ideal sebagai berikut: Hukum boyle dicetuskan oleh seorang ilmuwan asal inggris, yaitu robert boyle. N = m/mr sehingga persamaan gas ideal menjadi:
 Source: slideshare.net
Source: slideshare.net
Persamaan ini disebut hukum gas ideal atau persamaan keadaan gas ideal. Pada persamaan ini, p adalah tekanan absolut, t adalah temperatur absolut, dan v adalah volume spesifik. N = m/mr sehingga persamaan gas ideal menjadi: Persamaan ini merupakan pendekatan yang baik untuk karakteristik beberapa gas pada kondisi tertentu. P = tekanan gas (n/m 2) v = volume gas (m 3) n = jumlah mol (mol)
 Source: slideshare.net
Source: slideshare.net
Ternyata, ada beberapa hukum yang menjelaskan keterkaitan antara keempat besaran tersebut. Isometrik tekanan berbanding lurus dengan suhu. Hukum gas ideal (dalam jumlah mol) perbandingan di atas dapat diubah menjadi persamaan dengan memasukan jumlah mol (n) dan konstanta gas universal (r). Untuk gas nyata, nilai pv/nt sangat mendekati konstan sampai pada range tekanan yang besar, kita bisa melihatnya pada gambar (8.2). Van der walls adalah nama seorang fisikawan belanda, j.

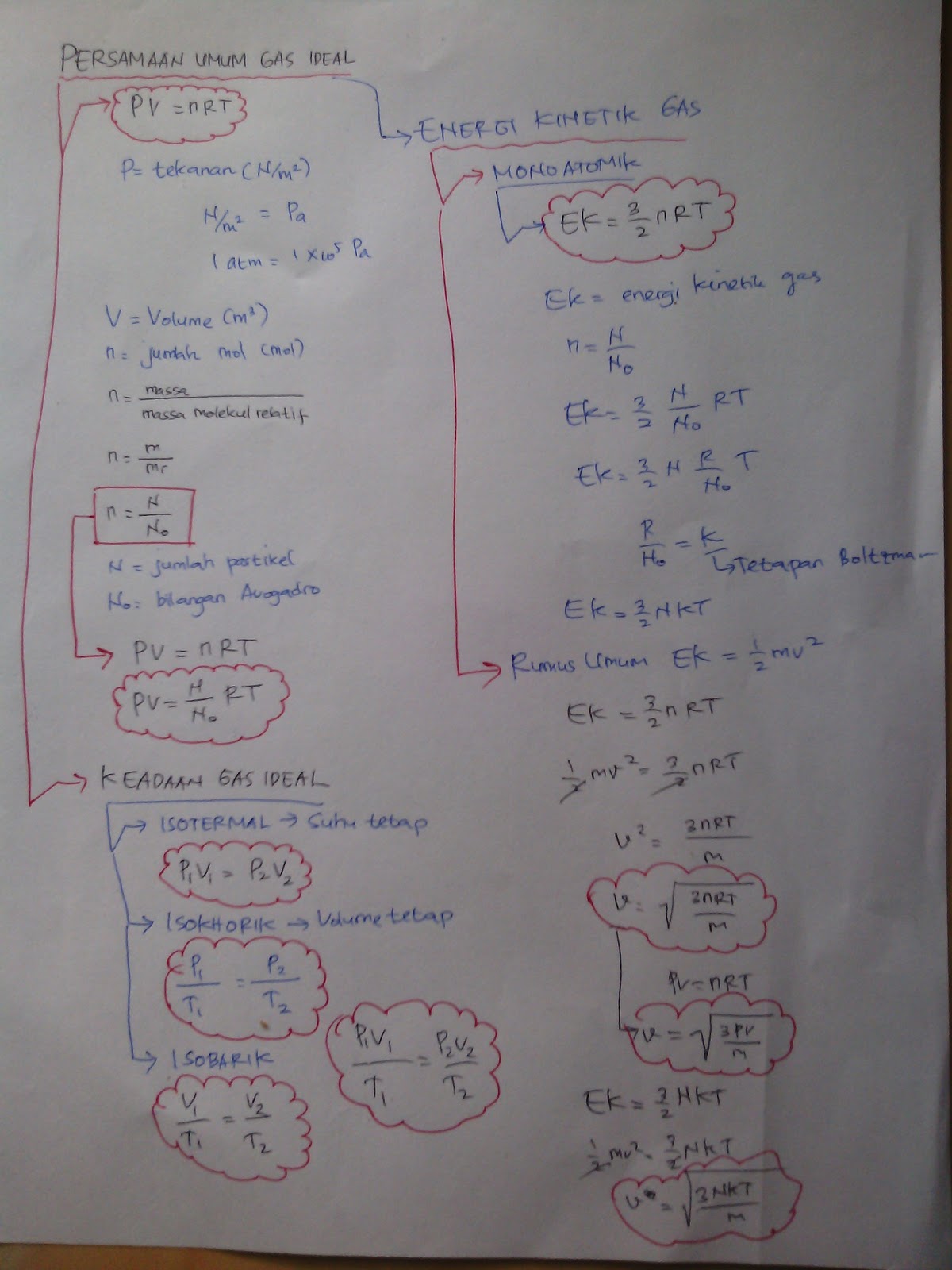
Massa jenis gas metana dalam tabung tertutup dapat dirumuskan dengan persamaan gas ideal seperti berikut: Persamaan umum gas ideal adalah persamaan yang menghubungkan antara tekanan (p), volume (v) dan suhu (t) sebuah gas. Persamaan ini disebut hukum gas ideal atau persamaan keadaan gas ideal. Tekanan gas pada keadaan 2 (n/m 2) v 1: Menunjukkan kaitan p dan v pada suhu tertentu.

Materi ini membahas tentang gas ideal dan termodinamika. P = tekanan gas (n/m 2) v = volume gas (m 3) n = jumlah mol (mol) P v = n r t. R= kna adalah konstanta gas umum, nilainya untuk semua gas adalah r = 8,314 j/mol. R = tetapan umum gas ideal (8,314 j/mol.k atau 0,082 l.atm/mol.k) r = 8,314 j/mol.k digunakan jika satuan tekanan dalam pascal (pa) dan volume dalam m 3.
 Source: slideserve.com
Source: slideserve.com
Gambar berikut merupakan kurva keadaan isoterm untuk tiap t pada gas ideal. Sebenarnya hukum avogadro menyatakan bahwa 1 mol gas ideal mempunyai volume yang sama apabila suhu dan tekanannya sama. Persamaan ini disebut hukum gas ideal atau persamaan keadaan gas ideal. P = r (t/v) pv = rt (1) dimana r adalah konstanta gas. P v = (m r t)/mr.

Untuk gas nyata, nilai pv/nt sangat mendekati konstan sampai pada range tekanan yang besar, kita bisa melihatnya pada gambar (8.2). Persamaan keadaan gas ideal pada ruang tertutup keadaan suatu gas ideal dipengaruhi oleh tekanan, suhu, volume dan jumlah molekul gas. Volume gas pada keadaan 1 (m 3) v 2: Ρ = m/v sehingga persamaan gas ideal menjadi. Pada ruang tertutup keadaan suatu gas ideal dipengaruhi oleh tekanan, suhu, volume dan jumlah molekul gas.
 Source: slideshare.net
Source: slideshare.net
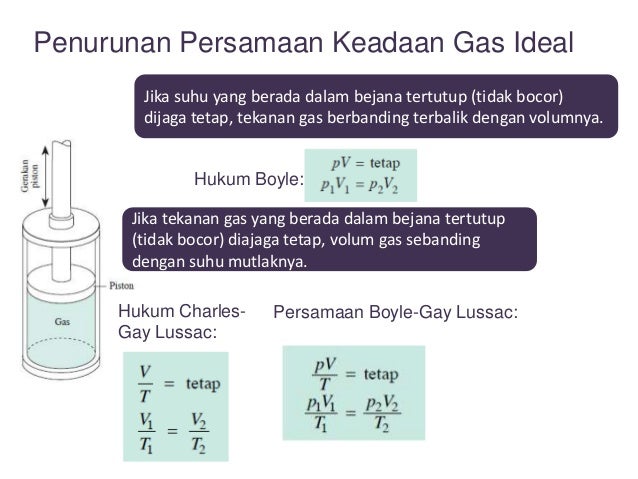
Pada suatu gas dalam jumlah mol (n) tertentu, maka persamaan keadaan gas idealnya adalah pv = nrt Semakin rendah tekanan gas pada temperatur tetap, semakin kecil deviasinya dari perilaku ideal. Hubungan antara suhu (t), tekanan (p) dan volume (v) tersebut dikenal dengan persamaan keadaan gas ideal. P 1 v 1 = p 2 v 2. Hukum boyle menyatakan bahwa tekanan gas berbanding terbalik dengan volume gas, saat temperatur dan jumlah zat gas dijaga tetap konstan.
 Source: bagicontohsoal.blogspot.com
Source: bagicontohsoal.blogspot.com
Jadi gas ideal memenuhi persamaan : Hukum boyle menyatakan bahwa tekanan gas berbanding terbalik dengan volume gas, saat temperatur dan jumlah zat gas dijaga tetap konstan. Artinya, semakin besar suhu maka tekanan semakin besar, dan v1 sebaliknya = t. Semakin tinggi tekanan gas, atau dengan dengan. Persamaan keadaan untuk gas dengan kerapatan rendah menjadi:
 Source: slideshare.net
Source: slideshare.net
Pada teori kinetik gas, keadaan gas diuji oleh beberapa ilmuwan dan menghasilkan beberapa temuan sebagai berikut: Ρ = (mr p)/(r t) ρ = (16 x 1,52 x 10 5)/(8310 x 298) ρ = 0,98 kg/m 3. Pertama, dalam penyelesaian soal, dirimu akan menemukan istilah stp. Ρ = m/v sehingga persamaan gas ideal menjadi. Massa jenis gas metana dalam tabung tertutup dapat dirumuskan dengan persamaan gas ideal seperti berikut:
This site is an open community for users to submit their favorite wallpapers on the internet, all images or pictures in this website are for personal wallpaper use only, it is stricly prohibited to use this wallpaper for commercial purposes, if you are the author and find this image is shared without your permission, please kindly raise a DMCA report to Us.
If you find this site beneficial, please support us by sharing this posts to your preference social media accounts like Facebook, Instagram and so on or you can also save this blog page with the title persamaan keadaan gas ideal by using Ctrl + D for devices a laptop with a Windows operating system or Command + D for laptops with an Apple operating system. If you use a smartphone, you can also use the drawer menu of the browser you are using. Whether it’s a Windows, Mac, iOS or Android operating system, you will still be able to bookmark this website.




