Kaidah Oktet. Caranya, dengan berusaha agar elektron terluar berjumlah 2 atau. Assalamualaikum.pada vidio kali ini dijelaskan materi ikatan kimia mengenai penyimpangan kaidah oktet, dimana senyawa tetap stabil meskipun tidak memiliki. Suatu senyawa mengikuti kaidah oktet apabila elektron terluar tiap unsurnya berjumlah 8, termasuk elektron yang diikat, sedangkan pada kaidah duplet elektron terluarnya berjumlah 2. Untuk itu ada beberapa pengecualian yang harus diperhatikan dalam menggambarkan struktur lewis molekul.
 Senyawa Kovalen Yang Mengalami Penyimpangan Kaidah Oktet From struktur.shareinspire.me
Senyawa Kovalen Yang Mengalami Penyimpangan Kaidah Oktet From struktur.shareinspire.me
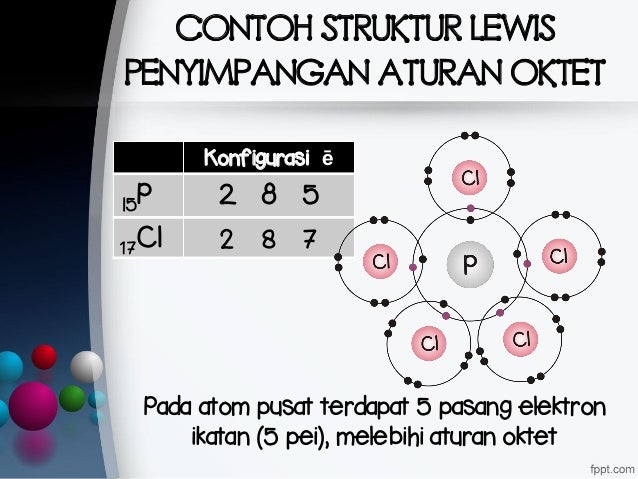
Senyawa dengan elektron valensi berjumlah lebih dari 8 dinamakan oktet berkembang. Dalam menentukan struktur lewis suatu senyawa, tidak harus mengikuti kaidah oktet (elektron valensi harus 8) atau kaidah duplet (2 elektron valensi), karena pada beberapa jenis unsur memiliki karakteristik yang berbeda. Aturan oktet adalah kecenderungan suatu atom di dalam molekul atau senyawa yang membentuk konfigurasi elektron seperti gas mulia (memiliki elektron valensi 8) sehingga suatu atom akan mengalami kondisi stabilnya. Penyimpang kaidah oktet berupa jumlah elektron terikat tidak sama dengan 8 atau lebih dari 8. Pada soal tersebut hanya gambar nomor (5) yang tidak mengikuti kaidah oktet maupun duplet. Pengecualian terhadap aturan oktet dibagi ke dalam tiga kategori yang ditandai dengan oktet tidak lengkap, jumlah elektron ganjil, atau lebih dari delapan elektron valensi di sekitar atom pusat.
Senyawa yang tidak mencapai aturan oktet.
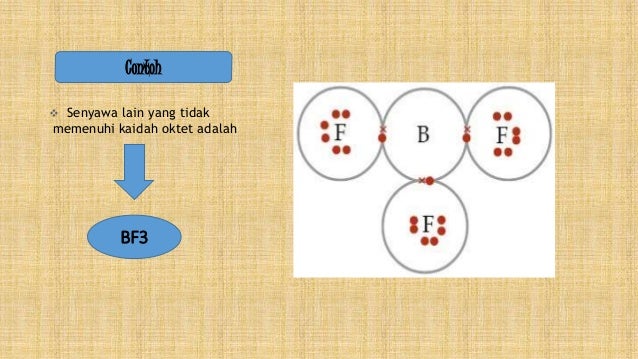
Materi ini bertujuan untuk memahami ikatan kimia dimana atom atom akan berikatan untuk mencapai kestabilan dengan prinsip kaidah oktet baik ikatan ion (elekt. Sedangkan unsur b mempunyai 7 elektron valensi sehingga membutuhkan 1 elektron lagi biar memenuhi kaidah oktet. Pengecualian kaidah oktet dibagi dalam tiga kelompok sebagai berikut: Untuk itu ada beberapa pengecualian yang harus diperhatikan dalam menggambarkan struktur lewis molekul. Aturan oktet adalah kecenderungan suatu atom di dalam molekul atau senyawa yang membentuk konfigurasi elektron seperti gas mulia (memiliki elektron valensi 8) sehingga suatu atom akan mengalami kondisi stabilnya. Caranya, dengan berusaha agar elektron terluar berjumlah 2 atau.
 Source: youtube.com
Source: youtube.com
Jumlah elektron valensi cl = 8 (memenuhi aturan oktet) jumlah elektron valensi b = 6 ( kuarang dari 8) sehingga tidak memenuhi aturan oktet; Senyawa yang tidak mencapai aturan oktet (oktet tidak sempurna) senyawa yang atom pusatnya mempunyai elektron valensi kurang dari 4 termasuk dalam kategori ini. Pembahasan soal kimia ujian nasional (un) 2016 no. Duplet adalah apabila atom memiliki 2 elektron di kulit terluarnya atau atom pusatnya dikelilingi 2 elektron (1 pasangan elektron). Pembahasan soal kimia un 2014 no.
 Source: belajaripa.net
Source: belajaripa.net
Pembahasan soal kimia un 2014 no. Sehingga konfigurasi elektron yang didapat akan sama dengan gas mulia yang stabil. Senyawa yang tidak mencapai aturan oktet (oktet tidak sempurna) senyawa yang atom pusatnya mempunyai elektron valensi kurang dari 4 termasuk dalam kategori ini. Penyimpangan kaidah oktet.cara mudah memperkirakan rumus kimia dan struktur lewis dari dua. Hal ini menyebabkan setelah semua elektron valensinya dipasangkan tetap belum mencapai oktet.
 Source: brainly.co.id
Source: brainly.co.id
Sehingga konfigurasi elektron yang didapat akan sama dengan gas mulia yang stabil. Duplet adalah apabila atom memiliki 2 elektron di kulit terluarnya atau atom pusatnya dikelilingi 2 elektron (1 pasangan elektron). Penyimpangan kaidah oktet.cara mudah memperkirakan rumus kimia dan struktur lewis dari dua. Pembahasan soal kimia un 2014 no. Aturan oktet adalah aturan yang menyatakan bahwa atom dari kelompok unsur utama cenderung berikatan dengan atom lain dengan cara memberi ataupun menerima elektron sedemikian rupa sehingga atom yang berikatan memiliki delapan elektron di kulit terluarnya.

Seperti yang disebutkan sebelumnya, aturan oktet berlaku terutama untuk unsur periode kedua. Pada kesempatan ini, kak ajaz hanya membahas satu paket soal saja karena 19 paket soal yang lain mempunyai tipe soal dan tingkat kesulitan yang sama. Penyimpangan kaidah oktet.cara mudah memperkirakan rumus kimia dan struktur lewis dari dua. Penyimpang kaidah oktet berupa jumlah elektron terikat tidak sama dengan 8 atau lebih dari 8. Pembahasan soal kimia un 2014 no.
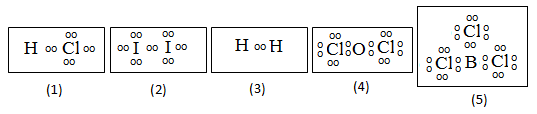 Source: sembilandewi.blogspot.com
Source: sembilandewi.blogspot.com
Jika kebetulan soal yang anda pegang saat ini sama dengan pembahasan ini, anda tinggal menyimak saja. Tentukan senyawa yang mengikuti kaidah oktet! Penyimpangan kaidah oktet.cara mudah memperkirakan rumus kimia dan struktur lewis dari dua. Dalam menentukan struktur lewis suatu senyawa, tidak harus mengikuti kaidah oktet (elektron valensi harus 8) atau kaidah duplet (2 elektron valensi), karena pada beberapa jenis unsur memiliki karakteristik yang berbeda. Seperti yang disebutkan sebelumnya, aturan oktet berlaku terutama untuk unsur periode kedua.
 Source: slideshare.net
Source: slideshare.net
Contohnya adalah becl 2, bcl 3, dan albr 3. Senyawa yang tidak mencapai aturan oktet (oktet tidak sempurna) senyawa yang atom pusatnya mempunyai elektron valensi kurang dari 4 termasuk dalam kategori ini. Penyimpang kaidah oktet berupa jumlah elektron terikat tidak sama dengan 8 atau lebih dari 8. Sedangkan unsur b mempunyai 7 elektron valensi sehingga membutuhkan 1 elektron lagi biar memenuhi kaidah oktet. Tentukan senyawa yang mengikuti kaidah oktet!
 Source: struktur.shareinspire.me
Source: struktur.shareinspire.me
Duplet adalah apabila atom memiliki 2 elektron di kulit terluarnya atau atom pusatnya dikelilingi 2 elektron (1 pasangan elektron). Dalam menentukan struktur lewis suatu senyawa, tidak harus mengikuti kaidah oktet (elektron valensi harus 8) atau kaidah duplet (2 elektron valensi), karena pada beberapa jenis unsur memiliki karakteristik yang berbeda. Unsur a mempunyai 5 elektron valensi sehingga membutuhkan 3 elektron lagi agar terpenuhi kaidah oktet. Pada soal tersebut hanya gambar nomor (5) yang tidak mengikuti kaidah oktet maupun duplet. Suatu senyawa mengikuti kaidah oktet apabila elektron terluar tiap unsurnya berjumlah 8, termasuk elektron yang diikat, sedangkan pada kaidah duplet elektron terluarnya berjumlah 2.
 Source: youtube.com
Source: youtube.com
Senyawa yang tidak mencapai aturan oktet (oktet tidak sempurna) senyawa yang atom pusatnya mempunyai elektron valensi kurang dari 4 termasuk dalam kategori ini. Untuk itu ada beberapa pengecualian yang harus diperhatikan dalam menggambarkan struktur lewis molekul. Pembahasan soal kimia un 2014 no. Namun, ada pengecualian atas kaidah ini. Soal kimia un 2014 terdiri dari 20 paket soal.
 Source: brainly.co.id
Source: brainly.co.id
Pada kesempatan ini, kak ajaz hanya membahas satu paket soal saja karena 19 paket soal yang lain mempunyai tipe soal dan tingkat kesulitan yang sama. Duplet adalah apabila atom memiliki 2 elektron di kulit terluarnya atau atom pusatnya dikelilingi 2 elektron (1 pasangan. Hal ini menyebabkan setelah semua elektron valensi dipasangkan tetap saja belum mencapai oktet. Dalam menentukan struktur lewis suatu senyawa, tidak harus mengikuti kaidah oktet (elektron valensi harus 8) atau kaidah duplet (2 elektron valensi), karena pada beberapa jenis unsur memiliki karakteristik yang berbeda. Tentukan senyawa yang mengikuti kaidah oktet!
 Source: slideshare.net
Source: slideshare.net
Jumlah elektron valensi cl = 8 (memenuhi aturan oktet) jumlah elektron valensi b = 6 ( kuarang dari 8) sehingga tidak memenuhi aturan oktet; Hal ini menyebabkan setelah semua elektron valensi dipasangkan tetap saja belum mencapai oktet. Hal ini menyebabkan setelah semua elektron valensinya dipasangkan tetap belum mencapai oktet. Penyimpang kaidah oktet berupa jumlah elektron terikat tidak sama dengan 8 atau lebih dari 8. Tentukan senyawa yang mengikuti kaidah oktet!

Tentukan senyawa yang mengikuti kaidah oktet! Seperti yang disebutkan sebelumnya, aturan oktet berlaku terutama untuk unsur periode kedua. Materi ini bertujuan untuk memahami ikatan kimia dimana atom atom akan berikatan untuk mencapai kestabilan dengan prinsip kaidah oktet baik ikatan ion (elekt. Jika kebetulan soal yang anda pegang saat ini sama dengan pembahasan ini, anda tinggal menyimak saja. Penyimpangan kaidah oktet.cara mudah memperkirakan rumus kimia dan struktur lewis dari dua.

Pengecualian kaidah oktet dibagi dalam tiga kelompok sebagai berikut: Hal ini menyebabkan setelah semua elektron valensi dipasangkan tetap saja belum mencapai oktet. Beberapa senyawa bersifat stabil meskipun tidak memenuhi kaidah, misalnya bf3. Pembahasan soal kimia un 2014 no. Senyawa yang atom pusatnya mempunyai elektron valensi kurang dari 4 termasuk dalam kelompok ini.
 Source: ruangguru.com
Pada soal tersebut hanya gambar nomor (5) yang tidak mengikuti kaidah oktet maupun duplet. Suatu senyawa mengikuti kaidah oktet apabila elektron terluar tiap unsurnya berjumlah 8, termasuk elektron yang diikat, sedangkan pada kaidah duplet elektron terluarnya berjumlah 2. Pengecualian terhadap aturan oktet dibagi ke dalam tiga kategori yang ditandai dengan oktet tidak lengkap, jumlah elektron ganjil, atau lebih dari delapan elektron valensi di sekitar atom pusat. Aturan / kaidah oktet menyatakan bahwa suatu unsur dikatakan stabil saat elektron valensinya 8 seperti golongan gas mulia (viiia). Contohnya adalah becl 2, bcl 3, dan albr 3.
 Source: lembaredu.github.io
Source: lembaredu.github.io
Soal kimia un 2014 terdiri dari 20 paket soal. Penyimpangan kaidah oktet.cara mudah memperkirakan rumus kimia dan struktur lewis dari dua. Pada umumnya, molekul yang mempunyai jumlah elektron valensi ganjil akan mempunyai susunan tidak oktet. Tentukan senyawa yang mengikuti kaidah oktet! Dengan demikian, senyawa yang terbentuk adalah ab 3.
 Source: berbagaistruktur.blogspot.com
Source: berbagaistruktur.blogspot.com
Dalam menentukan struktur lewis suatu senyawa, tidak harus mengikuti kaidah oktet (elektron valensi harus 8) atau kaidah duplet (2 elektron valensi), karena pada beberapa jenis unsur memiliki karakteristik yang berbeda. Dalam menentukan struktur lewis suatu senyawa, tidak harus mengikuti kaidah oktet (elektron valensi harus 8) atau kaidah duplet (2 elektron valensi), karena pada beberapa jenis unsur memiliki karakteristik yang berbeda. Jika kebetulan soal yang anda pegang saat ini sama dengan pembahasan ini, anda tinggal menyimak saja. Tentukan senyawa yang mengikuti kaidah oktet! Senyawa yang tidak mengikuti kaidah oktet atau duplet adalah nomor 5 bcl 3.
 Source: struktur.shareinspire.me
Source: struktur.shareinspire.me
Namun, ada pengecualian atas kaidah ini. Assalamualaikum.pada vidio kali ini dijelaskan materi ikatan kimia mengenai penyimpangan kaidah oktet, dimana senyawa tetap stabil meskipun tidak memiliki. Dalam menentukan struktur lewis suatu senyawa, tidak harus mengikuti kaidah oktet (elektron valensi harus 8) atau kaidah duplet (2 elektron valensi), karena pada beberapa jenis unsur memiliki karakteristik yang berbeda. Duplet adalah apabila atom memiliki 2 elektron di kulit terluarnya atau atom pusatnya dikelilingi 2 elektron (1 pasangan. Dengan demikian, senyawa yang terbentuk adalah ab 3.
 Source: ruangguru.com
Duplet adalah apabila atom memiliki 2 elektron di kulit terluarnya atau atom pusatnya dikelilingi 2 elektron (1 pasangan elektron). Sedangkan unsur b mempunyai 7 elektron valensi sehingga membutuhkan 1 elektron lagi biar memenuhi kaidah oktet. Hal ini menyebabkan setelah semua elektron valensi dipasangkan tetap saja belum mencapai oktet. Duplet adalah apabila atom memiliki 2 elektron di kulit terluarnya atau atom pusatnya dikelilingi 2 elektron (1 pasangan. Jumlah elektron valensi cl = 8 (memenuhi aturan oktet) jumlah elektron valensi b = 6 ( kuarang dari 8) sehingga tidak memenuhi aturan oktet;
 Source: lembaredu.github.io
Source: lembaredu.github.io
Materi ini bertujuan untuk memahami ikatan kimia dimana atom atom akan berikatan untuk mencapai kestabilan dengan prinsip kaidah oktet baik ikatan ion (elekt. Senyawa yang tidak mengikuti kaidah oktet atau duplet adalah nomor 5 bcl 3. Tentukan senyawa yang mengikuti kaidah oktet! Pembahasan soal kimia ujian nasional (un) 2016 no. Suatu senyawa mengikuti kaidah oktet apabila elektron terluar tiap unsurnya berjumlah 8, termasuk elektron yang diikat, sedangkan pada kaidah duplet elektron terluarnya berjumlah 2.
This site is an open community for users to do submittion their favorite wallpapers on the internet, all images or pictures in this website are for personal wallpaper use only, it is stricly prohibited to use this wallpaper for commercial purposes, if you are the author and find this image is shared without your permission, please kindly raise a DMCA report to Us.
If you find this site beneficial, please support us by sharing this posts to your own social media accounts like Facebook, Instagram and so on or you can also bookmark this blog page with the title kaidah oktet by using Ctrl + D for devices a laptop with a Windows operating system or Command + D for laptops with an Apple operating system. If you use a smartphone, you can also use the drawer menu of the browser you are using. Whether it’s a Windows, Mac, iOS or Android operating system, you will still be able to bookmark this website.





