Contoh Soal Hukum Faraday Kimia. 19 pembahasan kimia un 2017 no. M ni = 9,75 g Arus listrik 0,2 ampere dilewatkan selama 50 menit ke dalam sel elektrolisis yang mengandung larutan cucl 2. Soal kimia hukum faraday 1.

Contoh soal hukum faraday dan jawabannya. Soal #2 berapakah banyaknya gas hidrogen yang terbentuk dari elektrolisis larutan asam selama 5 menit dengan menggunakan arus listrik sebesar 965 ma? Massa ekivalen dari zn adalah….(ar zn = 65) a. Contoh soal hukum faraday i. 21 dan 23 pembahasan kimia un 2018 no. Kimia study center contoh soal dan pembahasan tentang perhitungan hukum faraday pada elektrolisis sma kelas 12 ipa.
Selanjutnya mari kita simak contoh soal hukum faraday 2 dan pembahasannya berikut ini.
Jika berat ekuivalen logam tembaga yaitu 635 dan berat ekuivalen gas oksigen yaitu 16 hitunglah besaran massa tembaga yang diendapkan pada katoda tersebut. Zn 2+ (aq) + 2e → zn (s) Contoh soal hukum faraday 1 1. Selanjutnya mari kita simak contoh soal hukum faraday 2 dan pembahasannya berikut ini. Soal #2 berapakah banyaknya gas hidrogen yang terbentuk dari elektrolisis larutan asam selama 5 menit dengan menggunakan arus listrik sebesar 965 ma? 4h + + 4e → 2h 2.
 Source: prima-iamcome.blogspot.com
Source: prima-iamcome.blogspot.com
Menentukan mol elektron dari elektrolisis h 2 so 4. Hukum faraday percobaan makalah penerapan dan contoh soal dosenpendidikancom hukum faraday menjelaskan tentang hubungan proses kimia dengan energi listrik. Itulah pembahasan lengkap tentang hukum, rumus dan contoh soal faraday, tentu saja semoga pembahasan ini bisa berguna dan bermanfaat bagi kalian para pembaca yang notabenya para pelajar indonesia. Contoh soal hukum faraday 2 dua buah elektrolisis, dengan sejumlah arus tertentu dalam waktu 2 jam dibebaskan 0,504 gram gas hidrogen ( ar h = 1). Soal kimia hukum faraday 1.
 Source: bagikancontoh.blogspot.com
Source: bagikancontoh.blogspot.com
Hitung massa perak yang mengendap pada katode. Bentuk contoh soal sel elektrolisis dan hukum faraday kimia kelas 12 sma/ma ini adalah pilihan ganda dengan lima alternatif jawaban dan sudah tersedia kunci jawabannya yang dapat di. Contoh soal hukum faraday dan pembahasan soal nomor 1. Sep 30 2020 contoh soal dan pembahasan hukum faraday kimia bagikan contoh zi6qenqy c7kgm. Contoh soal hukum faraday hukum 1 faraday hukum 1 faraday berbunyi, “ massa zat yang dihasilkan oleh suatu elektrode selama elektrolisis(w) akan berbanding lurus dengan jumlah muatan listrik yang akan digunakan (q) ”.
 Source: barucontohsoal.blogspot.com
Source: barucontohsoal.blogspot.com
Karena reaksi di katoda dikali 2, maka: Contoh soal hukum faraday dan pembahasan. 27 pembahasan kimia un 2019 no. Massa ekivalen dari zn adalah….(ar zn = 65) a. Apabila ukuran medan magnetik pada percobaan tersebut diperkecil menjadi ½ b dan luas permukaannya di perbesar menjadi 2 a.
 Source: lembaredu.github.io
Source: lembaredu.github.io
21 dan 23 pembahasan kimia un 2018 no. C sel elektrolisis dan hukum faraday dewita triani putri tembaga cu mempunyai ar 635. Contoh soal hukum faraday kimia. Contoh soal pembahasan sel volta bagian i 24082015. Contoh soal hukum faraday 1 (1) :
 Source: gambarsoalterbaru.blogspot.com
Source: gambarsoalterbaru.blogspot.com
Pada elektrolisis larutan niso 4 selama 45 menit menghasilkan endapan ni sebanyak 9,75 gram. Pada elektrolisis larutan niso 4 selama 45 menit menghasilkan endapan ni sebanyak 9,75 gram. M ni = 9,75 g 21 dan 23 pembahasan kimia un 2018 no. Reaksi elektrolisis h 2 so 4:
 Source: gurupaud.my.id
Source: gurupaud.my.id
Berapa gram kalsium yang dapat dihasilkan dari elektrolisis lelehan cacl 2 dengan elektroda grafit selama satu jam jika digunakan arus 10 a? Jika berat ekuivalen logam tembaga yaitu 635 dan berat ekuivalen gas oksigen yaitu 16 hitunglah besaran massa tembaga yang diendapkan pada katoda tersebut. Pada elektrolisis larutan znso 4 terjadi reduksi zn 2+ menjadi zn. 35 pembahasan kimia un 2015 no. 4h + + 4e → 2h 2.

W cu = (1/96.500) x i x t x me cu = dimana me = ar/biloks. Contoh soal hukum faraday dan pembahasan. Arus, i = 0,2 a; Berapa alumunium dapat diperoleh setiap jam jika digunakan arus 100 ampere. Sehingga jawaban dari pertanyaan berapa massa tembaga dari contoh soal rumus faraday diatas adalah sebesar 0,39 g tembaga.
 Source: berbagimengajar.blogspot.com
Source: berbagimengajar.blogspot.com
Pembahasan kimia un 2014 no. Contoh soal pembahasan sel volta bagian i 24082015. Contoh soal & pembahasan elektrolisis & hukum faraday sbmptn kimia sma soal no.1 (sbmptn 2017) elektrolisis 100 ml larutan cuso 4 0,1 m dalam bejana a dan 100 ml larutan agno 3 dalam bejana b dilakukan seri menggunakan arus tetap 1 a pada anoda dan katoda pt. Arus listrik 02 ampere dilewatkan selama 50 menit ke dalam sel elektrolisis yang mengandung larutan cucl 2. Hitung massa perak yang mengendap pada katode.
 Source: prima-iamcome.blogspot.com
Source: prima-iamcome.blogspot.com
4h + + 4e → 2h 2. Sebelumnya latihan soal senyawa hidrokarbon. Contoh soal hukum faraday akan dibahas secara lengkap dan ringkas oleh kursiguru pada kesempatan kali ini. Karena reaksi di katoda dikali 2, maka: Arus listrik 02 ampere dilewatkan selama 50 menit ke dalam sel elektrolisis yang mengandung larutan cucl 2.

Soal nomor 1 arus listrik sebanyak 9.650 c selama beberapa waktu dialirkan melalui 1 liter larutan perak nitrat 1 m dalam sebuah sel elektrolisis. Hitung massa perak yang mengendap pada katode. Hukum faraday adalah salah satu hukum yang menyatakan bahwa hubungan antara jumlah listrik yang dipakai dengan massa zat yang dihasilkan pada proses elektrolisis baik di katoda maupun anoda, dan teori faraday ini sering disebut juga dengan teori kuantitatif elektrolisis. Karena reaksi di katoda dikali 2, maka: 35 pembahasan kimia un 2015 no.
 Source: latihansoalyuk.blogspot.com
Source: latihansoalyuk.blogspot.com
Hukum faraday percobaan makalah penerapan dan contoh soal dosenpendidikancom hukum faraday menjelaskan tentang hubungan proses kimia dengan energi listrik. Massa ekivalen dari zn adalah….(ar zn = 65) a. 19 pembahasan kimia un 2017 no. 96.500 coulomb kemudian kita kenal dengan nama 1 f atau 1 faraday. Larutan asam mengandung kation h + katode (reduksi kation):
 Source: prima-iamcome.blogspot.com
Source: prima-iamcome.blogspot.com
Selanjutnya latihan uts sem 1 kimia kelas xii dengan pembahasan. 27 pembahasan kimia un 2019 no. Soal kimia hukum faraday 1. Diketahui i = 10 a; Apabila ukuran medan magnetik pada percobaan tersebut diperkecil menjadi ½ b dan luas permukaannya di perbesar menjadi 2 a.
 Source: teamhannamy.blogspot.com
Source: teamhannamy.blogspot.com
Hukum faraday adalah salah satu hukum yang menyatakan bahwa hubungan antara jumlah listrik yang dipakai dengan massa zat yang dihasilkan pada proses elektrolisis baik di katoda maupun anoda, dan teori faraday ini sering disebut juga dengan teori kuantitatif elektrolisis. Sebelumnya latihan soal senyawa hidrokarbon. 2h + + 2e → h 2 (x2) anoda : Reaksi elektrolisis h 2 so 4: Soal #2 berapakah banyaknya gas hidrogen yang terbentuk dari elektrolisis larutan asam selama 5 menit dengan menggunakan arus listrik sebesar 965 ma?
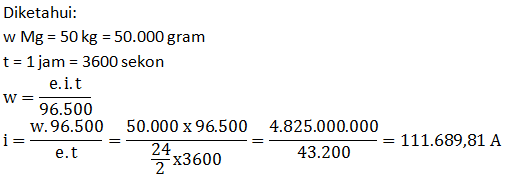 Source: latihansoalyuk.blogspot.com
Source: latihansoalyuk.blogspot.com
Massa ekivalen dari zn adalah….(ar zn = 65) a. Contoh soal hukum faraday 1 (1) : Perhatikan bagaimana cara menentukan massa ekivalen atau e dalam elektrolisis ini biloks unsur dan juga tetap diingat apa yang bereaksi di. Reaksi elektrolisis h 2 so 4: Massa ekivalen dari zn adalah….(ar zn = 65) a.

C sel elektrolisis dan hukum faraday dewita triani putri tembaga cu mempunyai ar 635. Hukum faraday sbmptn kimia sma soal no1 sbmptn 2017 elektrolisis 100 ml larutan cuso 4 01 m dalam bejana a dan 100 ml larutan agno 3 dalam bejana b dilakukan seri menggunakan arus tetap 1 a pada anoda dan. Alumunium diperoleh dari elektrolisis lelehan al 2 o 3. Hitung endapan cu, w cu, menggunakan rumus: Zn 2+ (aq) + 2e → zn (s)
 Source: bagikancontoh.blogspot.com
Source: bagikancontoh.blogspot.com
2h + + 2e → h 2 (x2) anoda : Reaksi elektrolisis h 2 so 4: Pembahasan soal sel elektrolisis dan hukum faraday yang lain bisa disimak di: 32 dan 33 pembahasan kimia un 2016 no. Pengertian hukum faraday dan bunyi hukum faraday.

C sel elektrolisis dan hukum faraday dewita triani putri tembaga cu mempunyai ar 635. Hitunglah endapan cu yang terbentuk pada katode. Karena reaksi di katoda dikali 2, maka: Contoh soal hukum faraday hukum 1 faraday hukum 1 faraday berbunyi, “ massa zat yang dihasilkan oleh suatu elektrode selama elektrolisis(w) akan berbanding lurus dengan jumlah muatan listrik yang akan digunakan (q) ”. Arus listrik 02 ampere dilewatkan selama 50 menit ke dalam sel elektrolisis yang mengandung larutan cucl 2.

Reaksi elektrolisis h 2 so 4: Contoh soal hukum faraday dan pembahasan. Contoh soal hukum faraday dan pembahasan. Reaksi elektrolisis h 2 so 4: W cu = (1/96.500) x i x t x me cu = dimana me = ar/biloks.
This site is an open community for users to do sharing their favorite wallpapers on the internet, all images or pictures in this website are for personal wallpaper use only, it is stricly prohibited to use this wallpaper for commercial purposes, if you are the author and find this image is shared without your permission, please kindly raise a DMCA report to Us.
If you find this site serviceableness, please support us by sharing this posts to your preference social media accounts like Facebook, Instagram and so on or you can also save this blog page with the title contoh soal hukum faraday kimia by using Ctrl + D for devices a laptop with a Windows operating system or Command + D for laptops with an Apple operating system. If you use a smartphone, you can also use the drawer menu of the browser you are using. Whether it’s a Windows, Mac, iOS or Android operating system, you will still be able to bookmark this website.




